Proteínas
¿Qué son?
Las proteínas son polímeros formados por aminoácidos en cadena que están unidos mediante enlaces peptídicos, los cuales poseen principalmente en su estructura al carbono, nitrógeno, oxígeno e hidrógeno; las proteínas son de suma importancia para los seres vivos porque existen una gran variedad de ellos, los cuales desempeñan funciones específicas y complejas para el adecuado funcionamiento de los organismos.
Acerca de los aminoácidos y enlaces peptídicos
Los aminoácidos son los monómeros de las proteínas, los cuales están estructurados en forma general por un carbono alfa el cual forma enlace con un grupo amino, un hidrógeno, un grupo carboxilo y una cadena lateral (radical); los radicales varían de acuerdo al aminoácido en cuestión, entre las que generalmente son veinte posibilidades para el radical que se une al carbono alfa, esto origina veinte aminoácidos los que abundan principalmente en los seres vivos, pero existen proteínas que tienen otros aminoácidos que son raros; los principales aminoácidos son la glicina, alanina, valina, leucina, isoleucina, fenilalanina, triptófano, serina, treonina, tirosina, prolina, hidroxiprolina, metionina, cisteína, cistina, lisina, arginina, histidina, ácido aspártico y ácido glutámico; éstos a su vez para los seres humanos se dividen en esenciales y los no esenciales, que no es más que los esenciales son los no que produce el cuerpo y por ende deben ser obtenidos a través de los alimentos y los no esenciales los produce el cuerpo a partir de los aminoácidos esenciales; algunos alimentos para el ser humano ricos en proteína son la carne de pollo, res, pescados y mariscos, frijoles, nueces y semillas, lácteos, legumbres, y cereales . Los aminoácidos son anfóteros cuando se encuentran en una disolución acuosa, es decir que dependiendo del pH pueden ionizarse como ácido o base, cuando se encuentran libres en un pH de 7 estos se encuentran ionizadas como acido y base, esto es, que el grupo amino posee una carga positiva y el grupo carboxilo una carga negativa, es decir que la molécula tiene dos polos (dipolo), lo que se conoce como zwiterión. Los enlaces peptídicos se forman entre la unión de el grupo carboxilo (-COOH) de un aminoácido más el grupo amino (-NH2) de otro aminoácido con la pérdida de una molécula de agua, esto hace que se formen dipéptidos (unión de dos aminoácidos), tripéptidos (tres aminoácidos) y polipéptidos (más de tres aminoácidos), en el enlace peptídico en la unión entre el carbono y el nitrógeno no hay libertad de rotación en la unión de estos dos grupos, mientras que los demás componentes de la molécula si lo tienen, tal enlace es estable en cambios del pH, sin embargo puede romperse por medio de hidrólisis o bien por acción enzimática, dicha unión entre aminoácidos está regulada por la información dada por los genes, en la que tres nucleótidos combinados (a lo que llamamos codón) designan un aminoácido, por lo que un gen designa un polipéptido, y cada polímero formado va a desempeñar una o más funciones específicas en el organismo, de acuerdo a la secuencia de aminoácidos que se formó.
ESTRUCTURAS DE LAS PROTEÍNAS
En el enlace peptídico que se forma durante la síntesis proteica, hay una secuencia de aminoácidos, lo cual establece la estructura primaria de la proteína, que a su vez va definiendo la estructura tridimensional que tendrá la molécula según la secuencia de aminoácidos, esta forma tridimensional indica la base de las estructuras secundarias, terciarias y cuaternarias de las proteínas, la secuencia de aminoácidos tiene una dirección que inicia con el extremo del grupo amino o terminal amino y finaliza con el extremo del grupo carboxilo o terminal carboxilo. La estructura secundaria es la forma de la proteína que se define en el espacio durante la síntesis proteica, lo cual puede presentarse en forma de espiral conocida como la hélice alfa que se representa en los esquemas con espirales o cilindros, o bien la forma plegada conocida como lámina beta la cual se representa en los esquemas con flechas planas en la que la punta de la flecha indica la terminal carboxilo; la forma de espiral se origina gracias a los puentes de hidrógeno entre un grupo carbonilo de un aminoácido y un grupo amino que se encuentra 4 unidades después en la secuencia de aminoácidos, en cambio las láminas beta tienen estos puentes de hidrógeno entre el grupo carboxilo de un aminoácido con un grupo amino que se encuentra en otro sitio diferente de la cadena polipeptídica que bien puede ser parte de la misma secuencia que se plegó sobre sí misma u otra que forma parte de una secuencia de aminoácidos diferente, las secuencias involucradas se les llama fibras beta, por lo que dependiendo de la dirección que tienen una con respecto a la otra se denomina, lamina beta paralela si tienen la misma dirección o bien, anti paralela si tienen dirección contraria. La estructura terciaria c ontiene además de puentes de hidrógeno, enlaces bisulfuros de grupos SH de aminoácidos de cisteína diferentes, uniones electrostáticas y fuerzas de Van der Waals, para darle estabilidad a la estructura, lo que le da una forma tridimensional globular (esférica), que contiene una zona que se encuentra más compacta donde pueden predominar laminas beta, hélices alfa o ambos, a la cual se le llama dominio. En la estructura cuaternaria contienen grupos prostéticos y cadenas polipeptídicas, los grupos prostéticos son porciones que no son proteínas que se encuentran ligadas a una proteína del tipo conjugada, en este tipo de estructura participan todos los tipos de enlaces que se mencionaron previamente para mantener la estabilidad de la estructura. Los enlaces que participan en estas estructuras que no son peptídicos pueden romperse más fácilmente que los enlaces peptídicos si se les aplican diversos cambios al medio en el que se encuentra la proteína, por ejemplo el calor y el pH, dicho cambio se le denomina desnaturalización, el cual puede ser irreversible.
ontiene además de puentes de hidrógeno, enlaces bisulfuros de grupos SH de aminoácidos de cisteína diferentes, uniones electrostáticas y fuerzas de Van der Waals, para darle estabilidad a la estructura, lo que le da una forma tridimensional globular (esférica), que contiene una zona que se encuentra más compacta donde pueden predominar laminas beta, hélices alfa o ambos, a la cual se le llama dominio. En la estructura cuaternaria contienen grupos prostéticos y cadenas polipeptídicas, los grupos prostéticos son porciones que no son proteínas que se encuentran ligadas a una proteína del tipo conjugada, en este tipo de estructura participan todos los tipos de enlaces que se mencionaron previamente para mantener la estabilidad de la estructura. Los enlaces que participan en estas estructuras que no son peptídicos pueden romperse más fácilmente que los enlaces peptídicos si se les aplican diversos cambios al medio en el que se encuentra la proteína, por ejemplo el calor y el pH, dicho cambio se le denomina desnaturalización, el cual puede ser irreversible.
Clasificación de las Proteínas
La composición de las proteínas las clasifica en simples o conjugadas, en las que las simples solo tienen en su estructura a los aminoácidos, mientras que las conjugadas tienen otros componentes que no son aminoácidos, es decir, los grupos prostéticos previamente mencionados, los componentes de las proteínas se separan mediante hidrólisis. Las proteínas simples pueden ser globulares o fibrosas, las fibrosas son mas resistentes a los factores que desnaturalizan a las proteínas; la proteínas globulares son las prolaninas (p. ej. Zeína que se encuentra en el maíz), la gluteninas (p. ej. Glutenina que se encuentra en el trigo), albuminas (p. ej. Seroalbúmina que se encuentra en la sangre), enzimas (p. ej. La insulina) y hormonas (p. ej. Hidrolasas); y las proteínas fibrosas son los colágenos (El tejido conjuntivo y cartilaginoso), elastinas (formaciones epidérmicas), queratinas (en los tendones y vasos sanguíneos) y fibroinas (p. ej. Hilos de seda de los insectos). Las proteínas conjugadas a su vez se dividen de acuerdo al grupo prostético al que se encuentre relacionado.
Otra forma de clasificar las proteínas es de acuerdo a la función que desempeña en el organismo de los seres vivos.
Enzimas: son aquellas que catalizan reacciones químicas en el organismo, es decir, aumentan la velocidad de la reacción. Por ejemplo la pepsina la cual cataliza la degradación de las proteínas de los alimentos en el estómago.
Proteínas estructurales: dan soporte y elasticidad a las estructuras en el organismo, algunos ejemplos son la tubulina que forma parte del citoesqueleto y el colágeno que se encuentra en tendones y huesos.
Proteínas almacenadoras: proporcionan almacen de nutrientes, por ejemplo la ferritina que almacena el hierro en el bazo.
Proteínas de transporte: son proteínas que se unen a iones o moléculas y los transportan. Ejemplo de ello es la hemoglobina que transporta el oxígeno de los pulmones a los tejidos.
Hormonas. Son proteínas que participan en la regulación del metabolismo en el cuerpo. Por ejemplo la insulina que regula el metabolismo de la glucosa.
Proteínas contráctiles o de movimiento coordinado: son proteínas que realizan contracciones y movimientos. Ejemplos son la actina y miosina que conforman a la contracción muscular.
Proteínas protectoras: algunas son muy específicas porque identifican a las sustancias extrañas para proteger el organismo contra ellos. Ejemplo los anticuerpos que inactivan a las proteínas extrañas que se encuentren en la sangre.
Toxinas: son proteínas que defienden el organismo contra otros. Por ejemplo la toxina botulínica que es venenosa contra organismos que no son Clostridium Botulinum.
Referencias
Bloomfield, M. (1992). Proteínas. Recuperado de https://anacanas.files.wordpress.com/2015/01/prot_bloomfield.pdf
Cañas, A. (2015). pequeñas moléculas. Recuperado de https://www.dropbox.com/s/90w5wdasi9g07xp/macromoleculas_Alberts_1_.pdf?dl=0
Geneser, F. (2007). HISTOLOGIA: Sobre bases biomoleculares. Buenos Aires, Argentina: EDITORIAL MEDICA PANAMERICANA.
González, J. (2015). FUNCIONES BIOLOGICAS DE LAS PROTEÍNAS. Recuperado de http://www.ehu.eus/biomoleculas/proteinas/prot3.htm
MedlinePlus. (2015). Proteína en la dieta. Recuperado de: http://www.nlm.nih.gov/medlineplus/spanish/ency/article/002467.htm
Terfloth, A. (2015). Composición química. Recuperado de: http://www.monografias.com/trabajos10/compo/compo.shtml
Wikipedia. (2015). Proteína. Recuperado de:http://es.wikipedia.org/wiki/Prote%C3%ADna
LIPIDOS
¿Qué son?
Son moléculas hidrofóbicas, es decir son insolubles en agua, por tener mayormente enlaces carbono-carbono, estos son enlaces no polares, y por lo tanto los lípidos también son compuestos orgánicos, por lo que son solubles en solventes orgánicos como el éter, benceno, etc., también están compuestos por hidrógeno y oxígeno en menor parte. Desempeñan en gran parte funciones como estructura en la membrana celular, también como reserva energética de las células animales y se almacenan en forma de aceites en las plantas.
Clasificación
Los lípidos se clasifican en dos grupos, los saponificables que contienen en su composición ácidos grasos y los no saponificables, los saponificables a su vez se dividen en simples y compuestos, en los que los simples solo se componen de carbono, hidrógeno y oxígeno, mientras que los compuestos además de estos componentes se agregan otros elementos como el azufre o biomoléculas como los hidratos de carbono. Entre los simples tenemos a los acilglicéridos (grasas y aceites) y en los compuestos tenemos a fosfolípidos (fosfoglicéridos y fosfoesfingolípidos) y glucolípidos (cerebrósidos y gangliósidos). Entre los no saponificables tenemos a los terpenoides y esteroides.
Acerca de los ácidos grasos
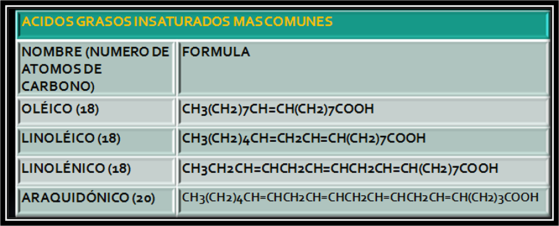
Las grasas son lípidos que como todos los demás contienen en su estructura a los ácidos grasos los cuales se forman por hidrólisis de los triacilgliceroles; los ácidos grasos son ácidos carboxílicos de cadena larga que pueden ser saturados e insaturados, es decir, que poseen enlaces dobles o triples entre sus enlaces carbono-carbono en el caso de los insaturados, que pueden tener mas de un doble enlace, siendo entonces poliinsaturados, los cuales se consideran como esenciales al no producirse fisiológicamente en el organismo de los animales, como los linoleicos o linolenicos. Los ácidos grasos saturados son flexibles a temperatura ambiente y también sólidos, mientras que los insaturados son rígidos en la región del doble enlace y se presentan en forma de líquidos aceitosos. Los ácidos grasos en general constan de un lado hidrofóbico que es no polar que es el extremo –COOH, y un lado hidrofílico que es polar, que es la cadena constituida por CH2 y al final CH3, esto significa que es una molécula bipolar o anfipática.
Los ácidos grasos de importancia biológica son monocarboxílicos, es decir, que tienen un grupo carboxilo, son cadenas de diversos tamaños, que pueden tener dobles enlaces.
En los ácidos grasos insaturados encontramos a los que han sido parcialmente hidrogenados formando a los ácidos grasos trans, con el fin de solidificarlas para utilizarlas en los alimentos; los ácidos grasos que han sido sometidos a hidrogenación parcial pueden cambiar de configuración cis a trans en el doble enlace a lo que se conoce como isomerización geométrica, o bien tener isomerización posicional lo cual indica que se cambió en la cadena de carbonos; recordemos que una configuración cis nos indica que los grupo funcionales se encuentran en el mismo lado del doble enlace, mientras que en la configuración trans los grupos funcionales se encuentran en lados opuestos del doble enlace; los ácidos grasos trans como el nombre lo indica tiene al menos un doble enlace en configuración trans, los mas frecuentes son los monoinsaturados, pero también hay diinsaturados con posiciones cis, trans o bien trans, cis, que en su mayoría los dobles enlaces se ubican en las posiciones 9 y 11; los ácidos grasos trans tienen impacto en la salud al estar ligadas a aumentar el riesgo de enfermedad coronaria y mayor riesgo de desarrollo de canceres; algunos productos que lo contienen son la margarina y algunas grasas de repostería.
Triacilgliceroles
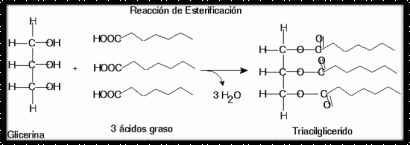
Los ácidos grasos se almacenan dentro de la célula de las plantas y animales, en forma de triacilglicéridos o triacilgliceroles, son lípidos saponificables simples, se almacenan como gotas de tamaño variable en los animales, que son los lípidos más abundantes, consta de tres cadenas de ácidos grasos unidas a un glicerol, formando enlaces de tipo ester, el cual se forma al reaccionar un ácido y un alcohol con la perdida de una molécula de agua por cada enlace. Los triacilgliceroles pueden ser simples que contienen un solo tipo de ácido graso, o bien, mixtos que contienen ácidos diferentes.
Fosfolípidos
Son compuestos que en el más frecuente de los casos, se une un glicerol con ácidos grasos en el carbono 1 y 2, mientras que en el tercero se une con un grupo fosfato que se une a un grupo hidrofílico, como la serina o etanolamina, lo que le da a la molécula la propiedad de ser anfipáticos, es decir, son parcialmente solubles en agua y en grasas, y además tiene la particularidad de de que forma parte importante de la estructura de la membrana celular, estos se agrupan formando una doble lámina a forma de un sándwich dejando el extremo hidrofílico en la superficie mientras que las colas se unen con otras entre las dos capas, formando la bicapa lipídica. Los fosfolípidos se dividen en dos: los fosfolípidos con glicerol previamente mencionado y los esfingolípidos, los cuales son fosfolípidos con esfongosina, en el que los ácidos grasos y el grupo fosfato no se unen al glicerol sino a la esfingosina; el más común es la esfingomielina, el cual forma parte de la estructura de la vaina de mielina que protege a los tejidos nerviosos, en el que un defecto puede causar patologías importantes como la de Niemmann.Pick y la esclerosis múltiple.
Glicolípidos
Son compuestos saponificables compuestos al igual que los fosfolípidos, pero en éstas moléculas en lugar de tener un grupo fosfato unido al alcohol (sea glicerol o esfingosina) se une un grupo hidrocarbonado (glúcido), que más frecuentemente es la galactosa. También son anfipáticos, e intervienen en la formación de membranas celulares, como los cerebrósidos que forman parte de las células cerebrales y nerviosas, en su estructura el alcohol al que se une es la esfingosina, alguna enfermedades relacionadas con la deficiencia de la formación de esta molécula son la enfermedad de Gaucher y la de Tay-Sachs.
Esteroides
Son lípidos no saponificables que derivan del fenantreno y tienen cuatro sistemas cíclicos de carbono; uno de los principales es el colesterol, un esterol, el cual forma parte de la formación de hormonas, vitamina D, etc., y constituye también en la estructura de la membrana celular, se sintetiza en las células a partir de acetil coenzima A, principalmente en el hígado, y se obtiene también a través de alimentos como huevo y carnes, se transporta en sangre como LBD (lipoproteína de baja densidad) que juegan un papel importante en patologías como la aterosclerosis. Los esteroides forman parte de vitaminas, fármacos, entre otros compuestos, de los más conocidos son la cortisona que es una hormona, la vitamina D2, la testosterona y progesterona que son hormonas sexuales masculino y femenino respectivamente.
Membrana celular
La membrana celular es una bicapa lipídica, es decir, tiene dos capas de fosfolípidos, además en su estructura también se encuentran proteínas, pero la proporción varía de acuerdo al tipo de célula, algunos lípidos que forman parte de la membrana celular son principalmente los fosfoglicéridos, los esfingolípidos, y colesterol, proporcionándole rigidez a la célula. 
Los glucolípidos desempeñan función como receptores en la membrana celular, es decir, a éstos se unen moléculas específicas como las hormonas. La membrana celular tiene la función de aislar la parte externa con la parte interna de la célula, es semipermeable, al no dejar entrar ni salir diversas moléculas, regulando el transporte de moléculas a través de ella, mantiene la forma de la célula, y contiene receptores para el adecuado funcionamiento de la célula.
Referencias
AvB. (2015). 1.- Estructura y característica de los ácidos grasos. Recuperado de:http://www.um.es/molecula/lipi01.htm
Bloomfield, M. (1992). lipidos. Recuperado de https://anacanas.files.wordpress.com/2015/01/lipidos_bloomfield.pdf
CAÑAS, A. (2009). Las funciones de los lípidos. Recuperado de http://cancerquest.org/index.cfm?page=37&lang=spanish
Cañas, A. (2015). pequeñas moléculas. Recuperado de https://www.dropbox.com/s/90w5wdasi9g07xp/macromoleculas_Alberts_1_.pdf?dl=0
FAO. (2015). ACIDOS GRASOS ISOMÉRICOS. Recuperado de http://www.fao.org/docrep/v4700s/v4700s0e.htm
Geneser, F. (2007). HISTOLOGIA. Buenos Aires, Argentina: PANAMERICANA.
González, J. (2015). FUNCIONES DE LOS LIPIDOS. Recuperado de http://www.ehu.eus/biomoleculas/lipidos/lipid2.htm
Vázquez, E. (2003). Tipos de lípidos. Recuperado de: http://laguna.fmedic.unam.mx/~evazquez/0403/tipos%20lipidos.html
Wikipedia. (2014). acido graso trans. Recuperado de http://es.wikipedia.org/wiki/%C3%81cido_graso_trans
Wikipedia. (2015). Lípido. Recuperado de: http://es.wikipedia.org/wiki/L%C3%ADpido